Blod, vävnader, celler och organ används i många medicinska behandlingar.
De kan rädda liv (t.ex. en blodtransfusion efter en olycka), förbättra livskvaliteten (t.ex. en njurtransplantation) eller skapa nytt liv (ägg- och spermiedonation och in vitro-befruktning).
Trots fördelarna med att använda ämnen av mänskligt ursprung finns det alltid risker, i synnerhet för sjukdomsspridning.
Kommissionen har därför fastställt höga kvalitets- och säkerhetsstandarder i enlighet med sitt uppdrag (artikel 168.4 a i fördraget om Europeiska unionens funktionssätt).
Dessutom arbetar kommissionen med att
- ta fram lagstiftning och riktlinjer
- hjälpa medlemsländernas myndigheter med genomförandet
- övervaka säkerheten och stödja projekt.
Det övergripande målet är att skydda människor.
Nya EU-regler om ämnen av mänskligt ursprung
Den 27 maj 2024 antog rådet den nya förordningen om kvalitets- och säkerhetsstandarder för ämnen av mänskligt ursprung avsedda för användning på människor.
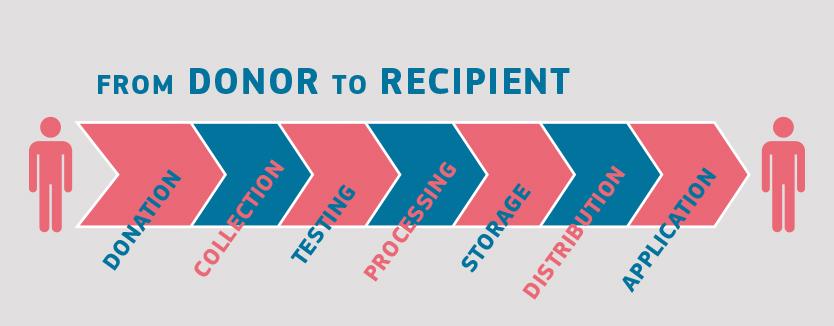
De olika stegen från givare till mottagare
Hanteringen av blod, vävnader, celler och organ följer alltid ungefär samma steg. Det börjar med donation och slutar med klinisk användning. Dessutom ingår testning av givare, tillvaratagande, bearbetning, distribution och ofta förvaring (särskilt för blod, vävnader och celler).
Allt detta görs på särskilda sjukvårdsinrättningar.
Samarbete
Tillsammans med Europarådet och EU:s smittskyddsmyndighet tar kommissionen fram praktiska riktlinjer för att hjälpa blodcentralerna att tillämpa reglerna.
Finansiering
Kommissionen är med och finansierar projekt som rör ämnen av mänskligt ursprung (humanmaterial).
Hälso- och sjukvården är dock ländernas eget ansvar och därför fattas alla beslut om metoder för ämnen av mänskligt ursprung på nationell nivå. Kommissionen har inget inflytande över besluten som kan se olika ut beroende på land.
De metoder som EU-länderna tillåter måste dock tillämpas i enlighet med EU:s krav på säkerhet och kvalitet.
Nationella myndigheter kan också välja att införa ännu strängare säkerhets- och kvalitetskrav, t.ex. ytterligare labbtest vid lokala utbrott av en mycket smittsam sjukdom.
Åtgärder under covid-19-pandemin
Covid-19-pandemin har varit en svår utmaning för folkhälsoarbetet. Flera initiativ har tagits för att förbättra och samordna insatserna.
- Kommissionen har bidragit till projekt för att tillvarata plasma från tillfrisknade covid-19-patienter.
- EU:s smittskyddsmyndighet (ECDC) har uppdaterat sin vägledning om covid-19 och ämnen av mänskligt ursprung.
- Kommissionen har publicerat en vägledning om plasma från tillfrisknade covid-19-patienter.
- Kommissionen har klargjort att ämnen av mänskligt ursprung är väsentliga varor och tjänster som måste kunna fortsätta att cirkulera fritt i EU.
Riktlinjer
Europarådet ser regelbundet över och uppdaterar de tekniska kraven i sina vägledningar och riktlinjer:
- Vägledning för beredning, användning och kvalitetssäkring av blodkomponenter
- Riktlinjer för god praxis för blodcentraler
- Vägledning om kvalitets- och säkerhetskrav för vävnader och celler som ska användas på människor
Europarådet tar också fram riktlinjer om olika aspekter som gäller humanmaterialets säkerhet och kvalitet.
ECDC gör riskbedömningar och tar fram beredskapsplaner vid utbrott av sjukdomar som kan spridas via blod, vävnader, celler och organ. De senaste gäller





