Un amplio abanico de terapias médicas recurren a la utilización de sangre, tejidos, células y órganos.
Los tratamientos basados en estas sustancias de origen humano (SoHO, por sus siglas en inglés, de «Substances of Human Origin») permiten salvar vidas (por ejemplo, mediante la transfusión de sangre en caso de traumatismo), mejorar la calidad de vida (gracias a los trasplantes de riñón u otros órganos) e, incluso, contribuir a la concepción (gametos y fecundación in vitro).
A pesar de estas ventajas, el uso de SoHO presenta riesgos, en particular de transmisión de enfermedades.
La Comisión Europea contribuye a controlar estos riesgos en virtud del mandato de establecer altos niveles de calidad y seguridad de las sustancias de origen humano que le confiere el artículo 168, apartado 4, letra a), del Tratado de Funcionamiento de la Unión Europea.
A tal fin, lleva a cabo una serie de actividades, entre las que se incluyen:
- elaboración de legislación y desarrollo de orientaciones
- ayudar a las autoridades nacionales en su aplicación
- actividades de vigilancia y apoyo a proyectos
El objetivo último es proteger a los ciudadanos.
Nuevas normas de la UE sobre sustancias de origen humano
En mayo de 2024, el Consejo adoptó el nuevo Reglamento sobre las normas de calidad y seguridad de las sustancias de origen humano destinadas a su aplicación en el ser humano.
La Junta de Coordinación de SoHO (JCS) creada por dicho Reglamento tiene por objeto garantizar procedimientos coherentes para la aplicación de este y de otra legislación pertinente de la Unión.
Organización del sector
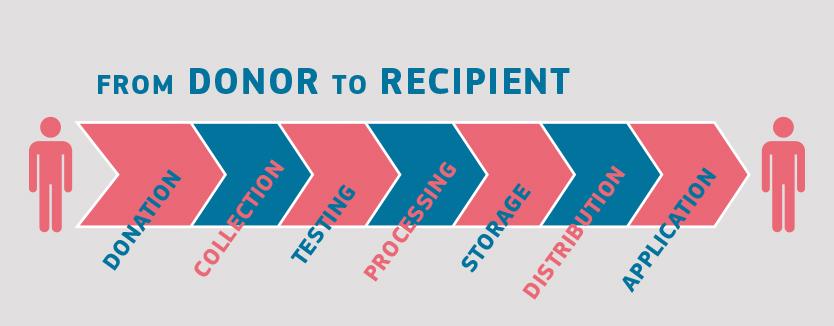
Aunque los donantes y los posibles receptores clínicos de sangre, tejidos, células y órganos son diferentes, la mayoría de las sustancias de origen humano siguen el mismo flujo de procesamiento: donación inicial, seguida de las fases de recogida, procesamiento y distribución, hasta culminar en la aplicación clínica. A esto se suman la realización de pruebas sobre los donantes y, con frecuencia, el almacenamiento de estas sustancias (en particular, en el caso de la sangre, los tejidos y las células).
Estas actividades se llevan a cabo en establecimientos médicos especializados.
Cooperación
La Comisión Europea colabora estrechamente con órganos especializados como el Consejo de Europa y el Centro Europeo para la Prevención y el Control de las Enfermedades en la elaboración de directrices prácticas que faciliten la aplicación de este marco legislativo vinculante en los centros de transfusión sanguínea.
Financiación de acciones
Además del trabajo habitual de la autoridad competente, la Comisión Europea financia acciones en el ámbito de las sustancias de origen humano.
Sin embargo, en la medida en que la asistencia sanitaria sigue siendo una competencia de los Estados miembros, las decisiones sobre las prácticas autorizadas para estas sustancias se toman a nivel nacional. La Comisión no interviene en esas decisiones, que pueden variar de un país a otro.
No obstante, una vez que los países de la UE autorizan sus prácticas, estas deben organizarse en consonancia con los requisitos legales de seguridad y calidad aplicables en la Unión.
Por su parte, las autoridades nacionales pueden optar por aplicar requisitos más estrictos de seguridad y calidad, como, por ejemplo, pruebas de laboratorio adicionales en respuesta a un brote epidemiológico local de una enfermedad altamente contagiosa.
Directrices
El Consejo de Europa revisa y actualiza periódicamente los requisitos técnicos en sus documentos siguientes:
- Guía para la preparación, uso y control de la calidad de los componentes sanguíneos
- Directrices de buenas prácticas para los centros de transfusión sanguínea
- Guía sobre calidad y seguridad de los tejidos y las células para su aplicación en el ser humano
Además, elabora directrices ad hoc sobre distintos temas relacionados con la seguridad y la calidad de las sustancias de origen humano (SoHO).
Tras la publicación del nuevo Reglamento sobre sustancias de origen humano (SoHO), el ECDC está elaborando activamente directrices técnicas sobre la prevención de la transmisión de enfermedades contagiosas a través de SoHO.
Además, en el caso de brotes de enfermedades infecciosas relacionadas con SoHO, el ECDC también publicará evaluaciones rápidas de riesgos con asesoramiento y recomendaciones para mantener la seguridad microbiana de las SoHO en el contexto de estos acontecimientos. Las publicaciones y actualizaciones recientes sobre las actividades del ECDC relacionadas con la seguridad microbiana de las SoHO se publican en el sitio web del ECDC.






